

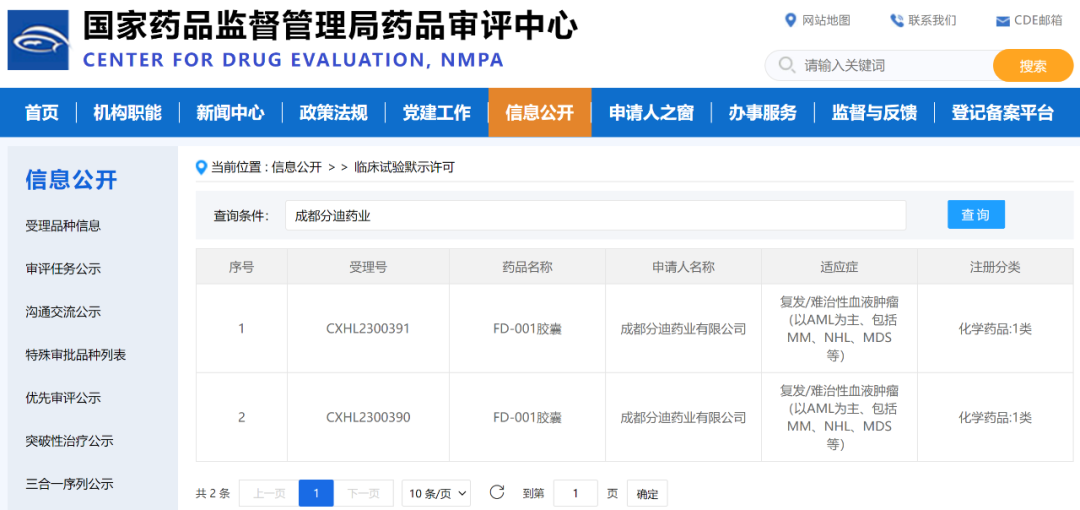
祝賀成都分迪藥業(yè)口服藥物FD-001于2023年6月26日順利獲得國家藥監(jiān)局的臨床試驗批準。成都分迪藥業(yè)自主研發(fā)的首個口服分子膠藥物FD-001實現(xiàn)了從PCC到獲臨床試驗默示許可僅11個月的“分迪速度”。
FD-001是利用分迪藥業(yè)專有的“ProDeDrug”分子膠合理設計平臺開發(fā)的一種口服分子膠藥物。FD-001擬用于急性髓系白血病(AML)、多發(fā)性骨髓瘤(MM)和非霍奇金淋巴瘤(NHL)等血液腫瘤的治療。
鈞慧生物有多項抗腫瘤藥物評價經(jīng)驗,實體腫瘤和血液腫瘤模型成熟,覆蓋各類型的抗腫瘤藥物評價。此外,鈞慧生物還提供抗腫瘤藥物體外藥效實驗。鈞慧生物一直致力于為客戶提供最好的藥物評價服務。